Artériás vérgáz elemzés – alapok

Az artériás vérgázok (ABG) meglehetősen megfélemlítőek lehetnek, különösen azoknak az ellátóknak, akik újak a kritikus ellátásban. Az alapelvei kétségtelenül összetettek, és sok kémiai reakciót foglalnak magukban – amelyek mindegyike nagyon fontos, de valószínűleg elsöprő, ha csak most kezdi megtanulni az értelmezését. Ennek a beszélgetésnek nem az a célja, hogy megtanítson mindent, amit a sav-bázis egyensúlyról és az vérgázról tudni lehet, hanem inkább funkcionális alapot nyújtani, amelyre ismeretét építheti. Tehát elhagyjuk a képzeletbeli egyenleteket (mínusz egy alapvetõ kémiai reakció) és a fodros tudományt, és megtanuljuk értelmezni az ASTRUP-kat azáltal, hogy felhasználjuk azokat a hozzáértõ nyomozói készségeket, amelyeket az alacsony költségvetésû detektívmûsorok nézése között eltöltött sok évében szerzett.
Alapvető élettan
A sejtlégzés – kérem, olvasson tovább, ígérem, nem beszélek a Krebs-ciklusról – minden életfenntartó biológiai folyamat magja. Energiát termel a szervezet számára, és kiegészíthető (aerob) vagy anélkül (anaerob) oxigénnel. Az aerob sejtlégzés kínálja a leghatékonyabb energiatermelést, mellyel víz és szén-dioxid (CO2) keletkezik melléktermékként. Anaerob sejtlégzés akkor következik be, amikor a sejtek oxigénfogyasztása meghaladja az oxigén rendelkezésre állását, kevesebb felhasználható energiát termel, és melléktermékként tejsav keletkezik.

A vér pH-jának belső egyensúlyát nagyrészt a szén-dioxid és a bikarbonát egyensúlya szabályozza. Az alveolusokban zajló gázcsere kivezeti az oxigénmolekulákat a belélegzett levegőből és a felesleges CO2 molekulákat a vénás vérből. A légzőrendszert az agyban található kemoreceptorok mozgatják, amelyek érzékenyek a CO2-koncentráció ingadozására. A megnövekedett CO2 a vérben megnövekedett perctérfogatot vált ki, hogy több CO2 ürüljön ki; fordítva, az alacsony CO2-koncentráció hipoventilációt vált ki a többlet megtartása érdekében. A visszatartott CO2 molekulák vízzel egyesülve szénsavat képeznek. A szénsav disszociál (szétszakad), és hidrogénionná (az acidózis előidézője) és bikarbonátionná (pH-puffer) válik. A bikarbonátot a vesék is figyelik és termelik, ha szükséges a hidrogénionok egyensúlyához. Egészséges betegeknél ez a mechanizmus a vér pH-ját 7,35 és 7,45 között tartja; azonban a normál fiziológia megzavarása felboríthatja ezt az egyensúlyt, és acidózishoz vagy alkalózishoz vezethet.
A sav-bázis zavarok négy fő típusa különböztethető meg, amelyek számos mögöttes patológiából származnak. A zavar típusától függetlenül a végső kezelés a kiváltó ok kezelése. A sav-bázis egyensúlyhiányt további tényezők bonyolíthatják, és időnként egynél több etiológia is hatással lehet a betegre. E megbeszélés céljaira a négy alaptípusnál maradunk:
o A respiratorikus acidózis a nem megfelelő alveoláris szellőzés következménye, ami megnövekedett CO2-visszatartáshoz vezet a véráramban. Ennek számos oka lehet, mint például a stroke, a központi idegrendszeri depresszió (opioid túladagolás stb.) és az olyan állapotokból eredő izomelégtelenség, mint a myasthenia gravis.
o A respiratorikus alkalózis valamilyen más patológiához kapcsolódó hiperventiláció eredménye. A légúti alkalózis központi okai közé tartozik a stroke, a traumás fejsérülés, a fájdalom, a szorongás, a szalicilátok és más méreganyagok. A hipoxia légúti alkalózist is okozhat, mivel a szervezet megkísérli növelni az oxigénfelvételt a megnövekedett perctérfogat révén, és véletlenül túl sok CO2-t bocsát ki. A hipoxiával összefüggő okok közé tartozik többek között a tüdőgyulladás és a tüdőembólia.
o A metabolikus acidózisnak négy elsődleges oka van: a sav túltermelése (anaerob sejtlégzés -> tejsavtermelés), a sav alulkiválasztása, a sav lenyelése és a bikarbonát elvesztése a vesén (tubuláris acidózis) vagy a GI-rendszeren keresztül (hasmenés).
o A metabolikus alkalózis másodlagosan léphet fel a hidrogénionok elvesztése miatt – ha nincs megfelelő hidrogénion a szénsav megkötéséhez és képzéséhez, a vér bikarbonátkoncentrációja a normál szint fölé emelkedhet. Hányás (gyomorsavvesztés), intracelluláris ioneltolódások, vese ionveszteség vagy hipovolémia következtében a hidrogénionok elvesztése és másodsorban a magas bikarbonátszintek előfordulhatnak.
Az ABG alkatrészei
A pH annak mértéke, hogy egy anyag mennyire savas vagy bázikus. A pH-hoz nincsenek mértékegységek. A skála 0-tól 14-ig terjed, ahol a 0 rendkívül savas, a 14 pedig rendkívül bázikus. Az általános kémiában a valódi semleges 7. Az emberi vér normál pH-tartománya enyhén alkalotikus, 7,35 és 7,45 között van. A 7,35 alatti vér pH-ja acidémiának, a 7,45 feletti pH-érték pedig alkalémiának minősül. Még az ezen a tartományon kívüli kis eltérések is jelentős fiziológiai zavarokhoz vezethetnek.
A pCO2 a vérben keringő szén-dioxid koncentrációja. A pCO2 normál tartománya 35-45 Hgmm; azok számára, akik ismerik az ETCO2 használatát, ez könnyen megjegyezhető. A CO2-visszatartás vagy a 45 Hgmm-nél nagyobb pCO2-szintek általában hozzájárulnak a savasság növekedéséhez – ez alól az egyik lehetséges kivétel a krónikus restriktív tüdőpatológiák, mint például a COPD vagy az emphysema, ahol a páciens szervezete idővel a pCO2-nál nagyobb pCO2-értékhez alkalmazkodott. tipikus normák. A túlzott CO2-kibocsátás, amelyet a 35 Hgmm-nél kisebb pCO2 tükröz, általában hozzájárul a lúgossághoz. Metabolikus zavar esetén a légzőrendszer megváltoztathatja a pCO2-t, hogy a pH-t a 7,35 és 7,45 közötti homeosztatikus tartományban tartsa.
A pO2 a vérben lévő oxigénmolekulák mértéke, normál tartománya 80-100 Hgmm. Noha a pO2 fontos a páciens oxigénellátásának hatékonyságának megértésében, és betekintést nyújthat abba, hogy más kórképek hogyan hatnak kölcsönhatásba a beteg anyagcserezavarával, itt nem fogunk sokat beszélni róla, mivel nem játszik nagy szerepet a pH-egyensúlyban. kizárólag.
Végül a HCO3- a bikarbonát ionok mértéke a véráramban. Ennek normál tartománya forrásonként kissé eltér, de általában valahol 22-26 mEq/L között van. A nem megfelelő bikarbonát szint acidózishoz, míg a túlzott mennyiségű bikarbonát ion alkalózishoz vezethet. Akárcsak a pCO2-t úgy állítják be, hogy kompenzálja az anyagcserezavarokat, a bikarbonát szintje ingadozhat légúti eredetű pH egyensúlyhiány esetén.

Alkalmazzuk ezt néhány példára lépésenkénti folyamatban. Itt veheted fel a nyomozósapkát. Az eset megoldásához mindössze három kérdésre kell válaszolnunk.
1. Milyen bűncselekményt követtek el? (acidózis vagy alkalózis)
2. Ki a tettes? (légzési vagy anyagcsere)
3. Valaki megpróbálta leplezni a bűncselekményt? (kompenzált vs nem kompenzált)
1. példa
1. Annak kiderítéséhez, hogy mikor történt a bűncselekmény – vagy zavarás – először nézze meg a pH-t. Ha kevesebb, mint 7,35 , akkor acidózis van a kezein. Ha nagyobb, mint 7,45 , az alkalózis . Látod, ez könnyű.
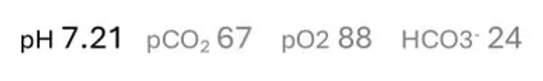
Mivel a pH 7,35 alatt van, ezt nyugodtan nevezhetjük acidózisnak .
2. Most keressük a tettest – melyik komponens, a pCO2 vagy a HCO3 konzisztens az acidózissal? Legközelebb a pCO2-t nézzük.

Ez a pCO2 meghaladja a normál 35-45 tartományt. TÚL SOK savas komponensünk van, ami megmagyarázza az alacsony pH-t (acidózis). Úgy tűnik, a pCO2 (légzési komponens) a tettes – úgy tűnik, hogy légúti acidózis van a kezünkön.
3. Végül, mivel tudjuk, hogy a légzőrendszer volt a hibás, ki kell derítenünk, hogy benne volt-e a bicarb is. Azaz – a bicarb azért változott, hogy megpróbálja kompenzálni a zavart? Értékeljük a HCO3-.

A HCO3- a normál tartományon belül van. Még nem nőtt, hogy kompenzálja a savfelesleget. Ezért ez egy kompenzálatlan légúti acidózis.
2. példa
Íme egy másik példa. Ugyanazt a 7,21-es pH-t használjuk – ez egy másik acidózis.

Ezúttal azonban a pCO2 normális, és nem korrelál az acidózissal. Úgy tűnik, a légzőrendszert meg lehet tisztítani ettől a bűncselekménytől… legalábbis egyelőre. Még egyszer rátérünk a bicarb-ra.

9-nél a bikarb jóval a normál tartomány alatt van. Mivel tudjuk, hogy a nem megfelelő mennyiségű bikarb hozzájárulhat az acidózishoz, ez magyarázza az alacsony pH-t. És – mivel a bikarbot ismerjük fel metabolikus komponensünknek – ezt nevezhetjük metabolikus acidózisnak. A kompenzált és a nem kompenzált érték meghatározásához mindössze annyit kell tennünk, hogy visszaugorjunk a pCO2-re. Mivel 37 Hgmm-nél a normál tartományon belül volt, ez egy kompenzálatlan metabolikus acidózis .
Még néhány példa a gyorstüzelésre

Ezt az ABG-t ugyanúgy lebontva, mint a többit, először azt vesszük észre, hogy a pH meghaladja a 7,45-et – ez alkalózis. De hú! A pCO2 magas, ami tulajdonképpen az acidózisnak felel meg , tehát tudjuk, hogy nem ez az oka egyensúlyhiányunknak. Ezt most hagyja figyelmen kívül – még mindig keressük a tettest.
32-nél a bicarb túlzottan bőséges, és összhangban van a pH-ban tükröződő alkalózissal. Ez azt jelzi , hogy metabolikus alkalózis áll mögöttünk . Most már van értelme a megnövekedett pCO2-nak – a szervezet további CO2-t tart vissza, hogy kompenzálja a magas bicarb-tartalmat. A légzőrendszer próbálja leplezni a bűncselekményt, de nem fejezte be teljesen a munkát, mivel a pH még mindig a normál tartományon kívül van. Ez egy részlegesen kompenzált metabolikus alkalózis. Oké, következő.

Ez a pH normális – tehát nincs mögöttes zavar, igaz? Ne olyan gyorsan, nyomozó.
Ugyanezt a lépésenkénti folyamatot követve észreveheti, hogy a pCO2 magas – extra sav van, és acidózisra számíthatunk. A bicarb is megemelkedett, így van extra alapunk is. Mivel mindkét összetevő a normál tartományon kívül esik, de a pH normális, tudjuk, hogy ez egy teljesen kompenzált ~valami.
Mivel a pH a normál alsó határán van (az acidotikus oldal felé hajlik – 7,40-et használhat középpontként, ha ilyen gázokkal foglalkozik), a legvalószínűbb, hogy a páciens mögött meghúzódó zavar inkább acidózis, mint alkalózis. Az emelkedett pCO2 az acidózisnak (a tettes) konzisztens érték, az emelkedett bicarb pedig magyarázza a kiegyensúlyozott pH-t (a fedőképességet); tehát ez egy teljesen kompenzált légúti acidózis. Akkoriban majdnem megúszták.
Záró gondolatok
Remélhetőleg ez az ostoba gyakorlat segített megérteni az ABG-t, és alapvető ismereteket szerezni a sav-bázis egyensúlyról. Még egyszer – szeretném hangsúlyozni, hogy ez csak a felszínt kaparja ezeknek a témáknak. A vérgázokat a betegellátás kiegészítőjeként kell használni , nem pedig a döntéshozatal egyetlen mozgatórugójaként. Bár a vérgázok hasznos eszközök lehetnek, kritikus fontosságú, hogy a szolgáltatók jó ítélőképességgel rendelkezzenek, és mérlegeljék az általános klinikai képet, mielőtt bármilyen kezelési döntést hoznának.
Hivatkozások
- Castro, Danny, and Michael Keenaghan. “Arterial Blood Gas.” National Library of Medicine, StatPearls Publishing, 8 Jan. 2024, www.ncbi.nlm.nih.gov/books/NBK536919/. Accessed 28 July 2024.
- Hopkins, Erin, et al. “Physiology, Acid Base Balance.” National Library of Medicine, StatPearls Publishing, 12 Sept. 2022, www.ncbi.nlm.nih.gov/books/NBK507807/. Accessed 28 July 2024.
- Burger M, Schaller DJ. Metabolic Acidosis. www.ncbi.nlm.nih.gov. Published July 17, 2023. https://www.ncbi.nlm.nih.gov/books/NBK482146/?report=reade
- Brinkman JE, Sharma S. Physiology, Metabolic Alkalosis. PubMed. Published July 23, 2023. Accessed August 8, 2024. https://www.ncbi.nlm.nih.gov/books/NBK482291/
- Brinkman JE, Sharma S. Physiology, respiratory alkalosis. Nih.gov. Published July 24, 2023. Accessed August 8, 2024. https://www.ncbi.nlm.nih.gov/books/NBK482117/
- Patel S, Sharma S. Respiratory Acidosis. National Library of Medicine. Published June 12, 2023. Accessed August 8, 2024. https://www.ncbi.nlm.nih.gov/books/NBK482430/
